mainmenu
- About Center
- Members
- Research
- Publications
- Facilities
- Super-depth Optical Imaging Lab
- Ultrafast Infrared Spectroscopy Lab
- Ultrafast IR-Visible Spectroscopy Lab
- Instrument and Chemistry Lab
- Molecular Imaging Lab
- Multidimensional Infrared Spectroscopy Lab
- Sample Preparation Lab
- Optical Frequency Comb Spectroscopy Lab
- Single Molecule Imaging Lab
- Spectroscopic Imaging Lab
- Theory and Computation
- Open Access Facility
- Collaborative Research Equipment
- Quantum Spectroscopy Lab
- Ultrafast Raman Probe Spectroscopy Lab
- Equipment Inventory
- Board
Board
News
고려대 연구팀, 325조 항암제 시장 '한획'..시스플라틴 작동원리 규명
고려대 연구팀, 325조 항암제 시장 '한획'..시스플라틴 작동원리 규명
국내 연구진이 2025년 약 325조원으로 성장할 것으로 전망되는 글로벌 항암제 시장에 한 획을 그었다. 홍석철 고려대학교 물리학과 교수가 이끈 연구팀은 다양한 암에서 널리 사용되는 항암제 ‘시스플라틴’의 작동원리를 분자 수준에서 규명해냈다. 과학기술정보통신부(과기정통부)에 따르면 연구팀이 작성한 ‘시스플라틴의 작용원리 규명’에 관한 논문은 24일 국제학술지 뉴클레익 애시즈 리서치에 게재됐다. 옥스퍼드대 출판부에서 발간하는 뉴클레익 애시즈 리서치의 영향력지수(Impact Factor)는 16.971점으로 핵산 분야 세계 최고 수준의 권위지로 꼽힌다.
연구팀이 시스플라틴의 작동원리를 규명한 방식은 다른 항암제에도 적용이 가능해 높은 시장성을 지닌 것으로 평가된다. 의약품 시장조사기관 아이큐비아(IQVIA)에 따르면 글로벌 항암제 시장은 연평균 9~12% 성장해 2025년에는 2730억달러(약 325조원)에 이를 것으로 전망된다. 항암제는 글로벌 의약품 소비규모 중 가장 큰 시장으로 보고되고 있다. 연구팀은 이 기술을 활용해 새로운 형태의 항암제를 디자인할 수 있을 것으로 전망했다. 또 DNA(데옥시리보핵산·생명체의 유전 정보를 담고 있는 화학 물질)를 표적으로 하는 항암제의 효능을 측정하는 데에도 해당 기술이 이용될 수 있다고 분석했다.
홍 교수 연구팀은 지난 2019년 9월부터 과기정통부의 개인기초연구 사업인 ‘중견연구자 지원’을 통해 이번 연구를 진행했다. 연구팀은 해당 연구의 주제·진행 계획 등을 직접 과기정통부에 제출, 평가를 받아 지원 대상자로 선정됐다. 중견연구자 지원 사업은 연구자 중심의 연구를 활성화하기 위해 도입된 제도다. 연구팀은 2022년 2월까지 지원을 받는다. 지금까지 약 2억5000만원이 해당 연구에 투입됐다.
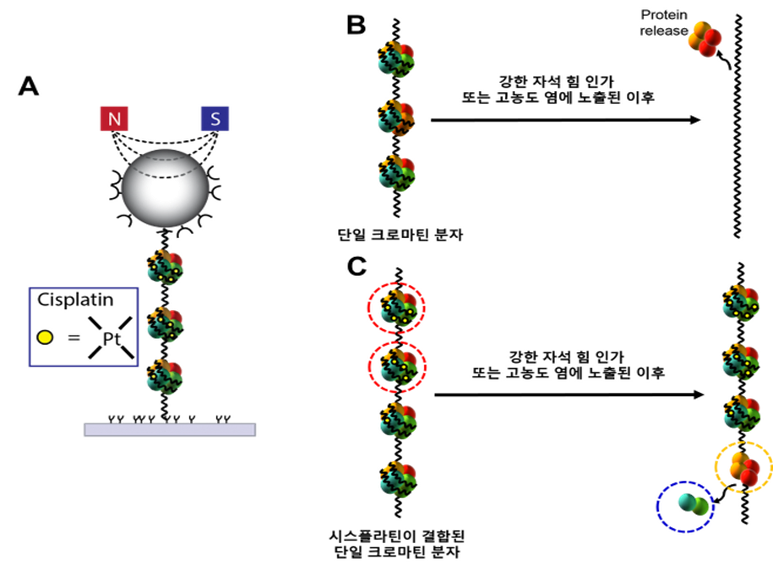
크로마틴 구조의 고정을 통한 시스플라틴의 항암 효과를 설명하는 물리적 모델. (A)는 자석 구슬에 부착된 단일 크로마틴 분자의 개략도. (B)는 인가된 힘과 고농도 염에 의해 붕괴되는 정상 단일 크로마틴 분자. (C)는 시스플라틴 결합에 의해 비가역적으로 고정된 단일 크로마틴 분자.(자료=홍석철 고려대학교 물리학과 교수)
1964년부터 의문으로 남았던 ‘시스플라틴의 비밀’ 풀다
시스플라틴은 미국의 생물물리학자 바넷 로젠버그가 1964년 전기장이 박테리아 성장에 미치는 영향을 연구하다 발견한 물질이다. 시스플라틴은 빠르게 분열하는 암세포 사멸에 탁월한 효과를 나타내는 것으로 확인되며 현재까지도 널리 사용되고 있다. 특히 고형암에 대한 뚜렷한 효과를 나타내는 시스플라틴의 발견은 ‘인류 암 정복의 전환점’이라 평가된다. 시스플라틴은 암 억제 효과가 높아 세계에서 널리 사용되고 있는 항암제지만, 작동원리에 대한 정확한 규명은 이뤄지지 않았던 물질이다. 연구팀은 시스플라틴이 인체 내 세포의 성장과 사멸 과정에서 크로마틴(chromatin·염색질)의 변화를 막아 항암효과를 낸다는 사실을 새롭게 규명했다. 암은 인체 내의 세포가 각종 원인에 의해 무제한 증식, 악성종양이 형성되는 질병이다. 시스플라틴은 이 같은 유전자 발현을 억제하면서 항암 효과를 냈다.
홍 교수는 전일 세종시 정부세종청사 과기정통부 브리핑실에서 이번 연구 성과에 대한 발표를 진행했다. 그는 “시스플라틴이 핵 속 DNA와 결합할 때 DNA의 구조를 변형시킨다는 사실이 기존 생화학 및 생물학적 연구 기법을 통해 잘 알려져 있었다”며 “그러나 실제 세포핵 속에 존재하는 크로마틴 구조에 대한 시스플라틴의 반응성과 구조 변형에 대한 이해는 미흡한 상태였다”고 설명했다.

홍석철 고려대학교 물리학과 교수가 세종시 정부세종청사 과학기술정보통신부 브리핑실에서 항암제 ‘시스플라틴’의 작동원리를 분자 수준에서 규명한 연구 성과에 대해 발표하고 있다.(사진=e브리핑 갈무리)
인체 내 세포의 생애주기는 크로마틴 구조가 느슨해지고 팽팽해지는 가역적인 새단장(리모델링) 과정을 통해 조절된다. 연구팀은 시스플라틴이 마치 접착제(fixer)처럼 작용해 크로마틴의 변화를 막아 항암효과를 낸다는 사실을 규명했다. 홍 교수는 “시스플라틴의 표적이 DNA 이중나선 사슬 자체라기보다 DNA의 세포 내 존재 형태인 크로마틴인 점을 실험적으로 밝혀냈다”고 설명했다.
시스플라틴의 결합에 따른 크로마틴 구조 및 물성 변화는 기존 생화학적 실험 방식에서는 파악하기 매우 어렵다. 크로마틴 크기가 매우 작기 때문이다. 인체의 유전정보가 담긴 DNA는 단백질 복합체를 중심으로 이중나선이 감긴 크로마틴 형태로 고도 압축돼 있다.
홍 교수는 연구 과정에 대해 “세포 내에 존재하는 DNA는 대부분 크로마틴 형태로 존재한다는 점에 주목했다”며 “크로마틴이 시스플라틴의 중요한 표적일 수 있다는 가능성을 바탕으로 시스플라틴이 크로마틴과 결합했을 때 크로마틴의 물성 변화를 분자 수준에서 정밀하게 측정했다”고 설명했다.
연구팀은 이를 통해 시스플라틴과 결합된 크로마틴은 영구적으로 탄력성을 잃는 것을 확인했다. 강하게 잡아당기는 물리적인 자극이나 고농도의 소금물 같은 화학적 자극에도 반응하지 않는 것으로 나타났다. 일반적인 크로마틴이 용수철처럼 가역적으로 리모델링되는 점과 확연하게 대조를 이뤘다. 연구팀은 크로마틴 변화를 분자 수준에서 실시간으로 포착하기 위해 ‘자성트위저 장비’를 사용했다. 이 장비는 단일 생체 분자 물성 측정 및 제어를 위해 쓰인다. 자석 간 인력을 이용해서 자석을 부착한 생체 분자에 힘을 가하는 방식으로 설계돼 있다.
연구팀은 실제 세포에서 추출한 크로마틴 형성 단백질을 이용해 시험관 내에서 크로마틴 분자를 형성했다. 이후 자체 개발한 기법을 통해 해당 물질 물성을 파악했다. 자성트위저를 이용해 크로마틴 분자 하나하나에 힘을 가하는 식으로 실험이 진행됐다.
홍 교수는 “DNA 사슬의 탄성을 측정하면 시스플라틴의 결합량을 잴 수 있다”며 “생체 환경과 유사한 염 농도 조건에서는 순수한 DNA 사슬에 시스플라틴이 결합하는 것이 현저히 억제됨을 확인할 수 있었다”고 설명했다.
연구팀은 시험관 내 리보핵산(RNA) 전사 실험을 통해 시스플라틴의 결합으로 고정된 크로마틴에서는 전사 효율이 뚜렷이 감소했다는 점을 확인했다. 세포 사멸에 관여하는 시스플라틴의 역할을 실험적으로 밝히는 데 성공한 것으로 평가되는 이유다.

자성트위저에 의한 단일 DNA 분자의 역학적 제어 설명 그림. (A)는 자석 구슬에 부착된 단일 DNA 분자의 개략도. (B)는 자성트위저에 의해 인가된 힘에 따른 DNA 분자 길이 변화 곡선.(자료=홍석철 고려대학교 물리학과 교수)
“항암제의 새로운 지평 연 연구”…향후 적용 범위 넓어
연구팀은 이번 연구를 통해 실제 생체 환경에서 시스플라틴이 크로마틴을 표적으로 강력한 항암효과를 낸다는 성과를 올렸다. 또 DNA 표적 기반 항암제의 개발과 효능 측정 장비로서 자성트위저를 제안했다는 점에서도 높은 평가를 받았다. 뉴클레익 애시즈 리서치의 게재를 결정한 옥스퍼드대 출판부 측은 이번 연구에 대한 평가를 진행하며 “항암제에 대한 새로운 사고의 지평을 연 연구”라고 했다.
홍 교수는 “이번 연구의 성과는 시스플라틴의 약리적 표적이 순수한 DNA라기보다는 보다 응축된 상위 구조인 크로마틴 형태일 수 있음을 제안한 것에 의의가 있다”며 “DNA를 표적으로 하는 다양한 항암제의 효능 측정과 작용원리 규명 및 강력한 항암제 디자인의 실마리가 될 것으로 기대된다”고 강조했다.
최근 개발된 다수의 항암제는 시스플라틴과 유사하게 핵 속 DNA를 표적으로 한다. 홍 교수는 “이번 연구는 항암제와 DNA 분자의 작용 원리를 밝히는 기초 연구에만 머물지 않고, 다양한 환경에서 항암제의 반응 효율을 조사하는 데 효과적인 방법을 제시함으로써 향후 유효 물질의 선정과 개발 과정에 유용하게 활용될 것으로 기대된다”고 말했다.
이번 연구는 홍 교수를 비롯해 △이남경 세종대학교 교수 △김재훈·송지준 한국과학기술원의 교수팀 △김준곤 고려대학교 교수팀과도 협력해 진행됐다. 이번 연구의 성과가 담긴 논문

항암제 ‘시스플라틴’의 작동원리를 분자 수준에서 규명한 연구 성과를 담은 논문의 공동 1저자인 박진성 박사(왼쪽)와 문현민 박사.(사진=과학기술정보통신부)